셀트리온 치료제 심사 결과 초읽기...국산 치료제 개발 현황은?
수정 2021-02-03 15:17:20
입력 2021-02-03 15:17:27
김견희 기자 | peki@mediapen.com
종근당·대웅제약, 셀트리온 이어 조건부 승인 신청 임박
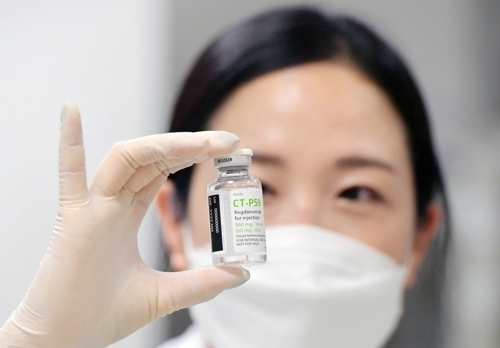
[미디어펜=김견희 기자]셀트리온이 개발한 신종 코로나바이러스(코로나19) 항체치료제 '렉키로나주(성분명 레그단비맙)'의 허가심사 결정이 코앞으로 다가오면서 국산 1호 치료제 탄생에 대한 기대감이 높아지고 있다.
 |
||
| ▲ 셀트리온 항체치료제 '렉키로나주'./사진=연합뉴스 | ||
3일 제약·바이오 업계에 따르면 식품의약품안전처는 오는 5일 셀트리온의 항체치료제 허가 여부를 최종적으로 결정하는 최종점검위원회를 연다. 이는 식약처가 코로나19 치료제 허가심사를 위해 마련한 전문가 자문 3중 절차의 마지막 단계다. 즉 렉키로나주가 최종점검위원회에서 허가를 확정하면 첫 국산 코로나19 치료제가 된다.
최종점검위원회에서는 회의를 통해 앞서 검증자문단과 중앙약사심의위원회 전문가 의견과 효능·효과, 권고사항 등을 종합적으로 살펴본다. 결과는 회의 당일 공개된다.
앞서 열린 검증 자문단과 중앙약사심의위원회에 참가한 전문가들은 모두 렉키로나주에 대해 임상 3상 시험을 전제로 허가가 가능하다는 의견을 낸 바 있다.
단 두 전문가 집단은 렉키로나주 투여 범위에 대한 의견은 달랐다. 중앙약심 전문가 집단은 경증 환자에 대한 임상적 의미를 도출할 수 없다고 판단하고 투여 대상자를 '고위험군'으로 제한했다. 반면 검증 자문단은 경증 및 중등증 코로나19 성인 환자에 렉키로나주를 투여해도 된다고 봤다.
셀트리온에 이어 코로나19 치료제 국산 2호가 될 것으로 점쳐지는 종근당의 '나파벨탄'은 조건부승인 신청이 당초 계획보다 지연되고 있다. 종근당 관계자는 "러시아에서 진행한 임상 2상 데이터 자료가 아직 도착하지 않은 것"이라며 "임상 자체에는 문제가 없다"고 설명했다. 이어 "데이터를 확보하는대로 식약처에 조건부 승인 신청을 할 계획"이라고 덧붙였다.
만약 이달 중으로 승인 신청이 이뤄진다면 이르면 내달 중으로 심사 결과가 나올 것으로 보인다. 회사는 심사 결과가 긍정적일 경우 나파벨탄이 중증 고위험군 환자를 위한 코로나19 치료제로 쓰일 것으로 회사는 기대하고 있다.
종근당은 지난해 8월 러시아 보건부로부터 임상 2상을 승인 받아 9월 25일부터 임상을 진행했다. 현재 멕시코와 세네갈에서도 임상 2상 시험을 진행 중이며 호주에서는 코로나19 종식을 위한 글로벌 임상시험 프로젝트인 'ASCOT' 임상에 참여해 대규모 임상 3상에 돌입했다.
종근당에 이어 임상 2/3상을 진행 중인 대웅제약의 '호이스타정', 임상 2상 완료 후 결과를 분석 중인 GC녹십자의 혈장치료제 역시 올 1분기 내 조건부허가를 신청할 계획인 가운데 상반기 내 심사 결과를 받을 수 있을 것으로 보인다.
대웅제약의 호이스타정은 만성 췌장염 등에 주로 쓰이는 전문의약품으로, 셀트리온에 이어 개발 중인 국산 치료제 중 유일하게 임상 3상에 진입했다. 이 약물은 경구제로, 만약 코로나19 치료제 개발에 성공할 시 치료 편의성이 증대될 것으로 기대된다.
GC녹십자는 코로나19 중증 환자를 위한 혈장치료제 'GC5131A'을 개발 중이며 코로나19 환자 60명을 대상으로 임상 2상 시험을 완료했다. 현재 임상 결과를 분석 중이며 이를 바탕으로 1분기 내 식약처에 조건부 허가 신청을 한다는 계획이다.
이밖에도 부광약품, 신풍제약, 동화약품, 엔지켐생명과학도 각 사 품목의 2상을 진행하고 있다.
[미디어펜=김견희 기자] ▶다른기사보기 


